Exercícios sobre isomeria óptica (com gabarito resolvido)
A isomeria óptica é um fenômeno da química orgânica que envolve moléculas que desviam a luz polarizada. Esse tipo de isomeria está diretamente ligado à presença de carbono quiral. Estudar seus conceitos é essencial para compreender propriedades químicas e biológicas de diversas substâncias. Pratique os seus conhecimentos com as questões abaixo.
Questão 1
Um paciente foi diagnosticado com uma infecção bacteriana e recebeu a prescrição do antibiótico cloranfenicol. O medicamento genético utilizado é uma mistura racêmica. Sobre essa mistura, é correto afirmar que:
a) É opticamente inativa por ser composta por moléculas aquirais.
b) É formada por quantidades iguais dos dois enantiômeros do fármaco.
c) Possui atividade biológica dobrada, pois contém ambas as formas dextrogira e levogira.
d) Apresenta um plano de simetria interno que cancela sua atividade óptica.
e) Deve ser administrada com cuidado, pois o enantiômero levogiro é sempre tóxico.
Resposta: alternativa B.
Uma mistura racêmica é definida como uma mistura equimolar (50% de cada) dos enantiômeros dextrogiro (+) e levogiro (–) de uma substância quiral. Como os desvios ópticos de cada um são iguais em módulo, mas em direções opostas, o efeito líquido é que a mistura é opticamente inativa.
Questão 2
A talidomida foi um medicamento amplamente receitado para grávidas nas décadas de 1950 e 1960 como sedativo e para combater enjoos. No entanto, causou graves malformações congênitas em milhares de bebês. Estudos posteriores mostraram que:
a) A talidomida não podia ser isolada separada por conta da racemização
b) O composto comercializado era um enantiômero puro, o que potencializou seu efeito tóxico.
c) A talidomida é um composto aquiral e, portanto, não possui isomeros ópticos.
d) A talidomida sofre racemização in vivo, tornando ineficaz a administração de um único enantiômero.
e) O problema ocorreu devido à baixa pureza óptica do fármaco produzido na época.
Resposta: alternativa D.
Este é o ponto crucial da tragédia da talidomida. Inicialmente, acreditava-se que apenas um dos enantiômeros era teratogênico (causador de malformações). Porém, descobriu-se que, no organismo humano, os enantiômeros da talidomida se interconvertem rapidamente (racemização). Portanto, mesmo administrando apenas o enantiômero considerado seguro, o corpo acaba produzindo a mistura racêmica, incluindo a forma tóxica.
Questão 3
O ácido láctico é uma molécula quiral formada durante a atividade muscular intensa. Ao analisar uma amostra de ácido láctico isolado de uma cultura de iogurte, um químico observou que ela desvia o plano da luz polarizada para a direita. Essa amostra é corretamente classificada como:
a) Um mistura racêmica de ácido lártico.
b) Um enantiômero levogiro.
c) Uma substância meso.
d) Um enantiômero dextrogiro.
e) Um composto opticamente inativo.
Resposta: alternativa D.
A nomenclatura é direta: uma substância que desvia o plano da luz polarizada para a direita (sentido horário) é denominada dextrogira e é identificada pelo sinal (+).
Questão 4
O limoneno é uma molécula quiral presente na casca de frutas cítricas. O enantiômero R-limoneno, encontrado na laranja, possui odor cítrico característico. Já o enantiômero S‑limoneno, encontrado no limão, possui odor semelhante, porém discernivelmente diferente.
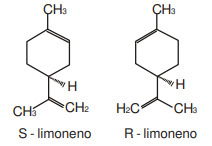
Essa diferença de odor entre os enantiômeros evidencia que:
a) As propriedades físicas dos enantiômeros sempre diferem significativamente.
b) Os receptores olfativos no nariz humano são ambidestros (reagem igualmente a ambos).
c) Os receptores olfativos no nariz humano são quirais, podendo diferenciar os enantiômeros.
d) O (–)‑limoneno é a forma mais estável termodinamicamente.
e) A mistura racêmica do limoneno possui um odor intermediário entre o de laranja e limão.
Resposta: alternativa C.
Esta questão aborda uma diferença de propriedade biológica entre enantiômeros. Enquanto a maioria das propriedades físicas e químicas (em ambientes aquirais) são idênticas, as propriedades biológicas são frequentemente diferentes. Isso ocorre porque os sítios de ligação em enzimas e receptores (como os olfativos) são ambientes quirais. Assim, os dois enantiômeros "se encaixam" de maneira diferente no receptor, gerando respostas sensoriais distintas.
Questão 5
O carvão ativado é comumente utilizado em campanhas de saúde para casos de intoxicação, pois adsorve uma série de toxinas no trato gastrointestinal. Se uma pessoa ingerir uma overdose de um fármaco quiral na forma de um enantiômero puro, o carvão ativado será capaz de adsorvê-lo porque:
a) O carvão ativado é quiral e interage seletivamente com a molécula do fármaco.
b) O carvão ativado é aquiral e, portanto, interage igualmente com ambos os enantiômeros.
c) O fármaco sofre racemização rápida no estômago antes da adsorção.
d) A adsorção é um processo físico que não depende da quiralidade do fármaco.
e) A superfície do carvão ativado contém centros quirais que adsorvem especificamente a forma tóxica.
Resposta: alternativa D.
O carvão ativado adsorve moléculas principalmente por forças inespecíficas, como interações de van der Waals. Como essas forças não dependem da geometria espacial quiral da molécula, o carvão ativado (que tem uma superfície aquiral) adsorve ambos os enantiômeros com a mesma eficiência. A adsorção é um fenômeno físico, não um reconhecimento molecular específico.
Questão 6
A molécula do ácido tartárico, encontrado em uvas, possui dois carbonos assimétricos. Uma de suas formas isoméricas, conhecida como ácido mesotartárico, é opticamente inativa.
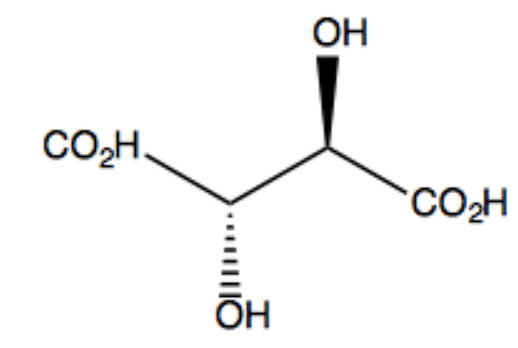
Isso ocorre porque essa molécula:
a) É um composto aquiral, sem carbonos assimétricos.
b) Forma uma mistura racêmica externa, neutralizando o desvio.
c) Apresenta um plano de simetria que torna a molécula superponível à sua imagem especular.
d) Sofre mutarotação rapidamente em solução, equilibrando os enantiômeros.
e) Possui os dois carbonos assimétricos com configurações iguais, mas a cadeia é simétrica.
Resposta: alternativa C.
Esta é a definição clássica de um composto meso. A molécula do ácido meso-tartárico possui dois carbonos assimétricos, mas eles possuem configurações opostas (um R e um S). Assim, enquanto parte da molécula desvia a luz para a direita, outra desvia a luz para a esquerda, anulando uma a outra.
Questão 7
Um técnico de laboratório identificou um composto com 16 isômeros opticamentes ativos. Assinale a alternativa que apresenta este composto:
a) 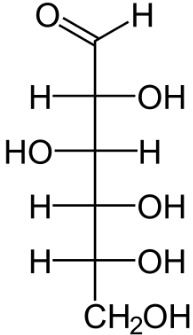
b) 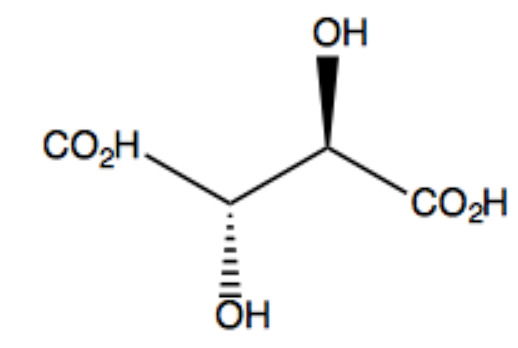
c) 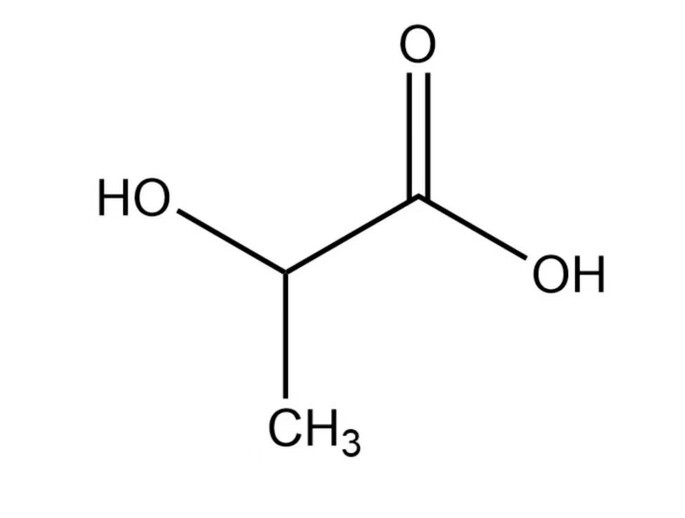
d) 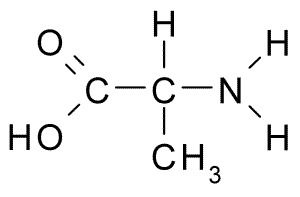
e) 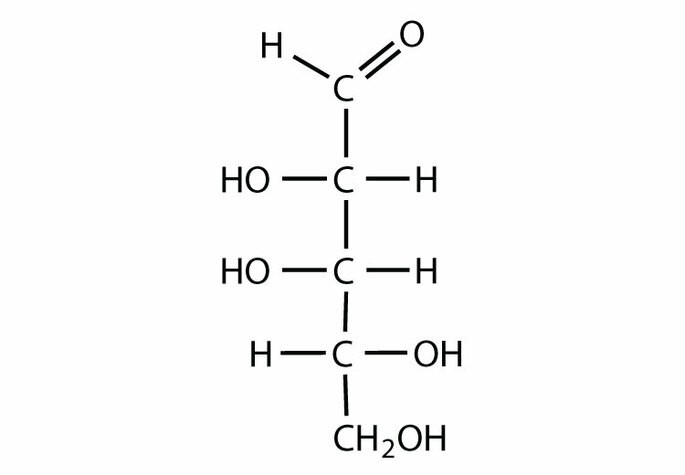
Resposta: alternativa A.
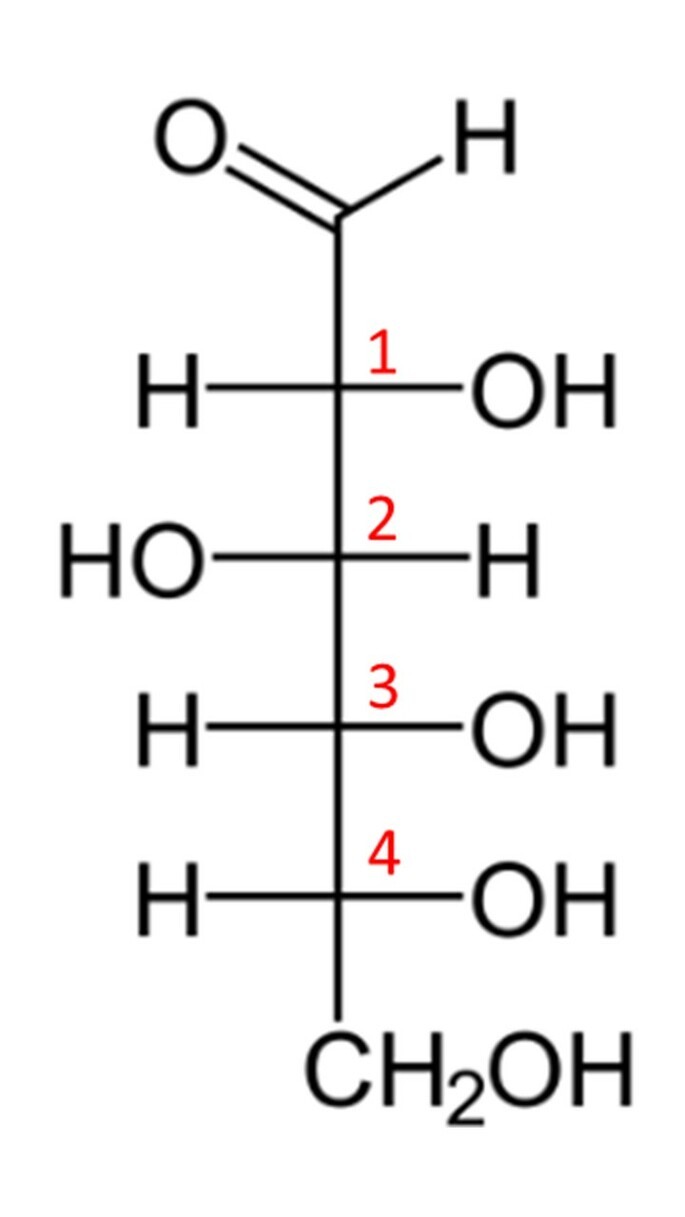
Podem ser identificados 4 carbonos quirais na molécula (destacados a seguir).
Assim,
Faça mais exercícios sobre isomeria:
Exercícios sobre isomeria plana (com gabarito explicado)
Exercícios sobre isomeria geométrica (com respostas resolvidas)
Continue estudando sobre isomeria:
Isomeria: o que é e seus tipos (com mapa mental)
Exercícios sobre isomeria óptica (com gabarito resolvido). Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/exercicios-sobre-isomeria-optica-com-gabarito-resolvido/. Acesso em:

