Exercícios para o ENEM (172)
Foram encontradas 6013 questões
GIRARDI, E. P Atlas da questão agrária brasileira. Disponível em:...
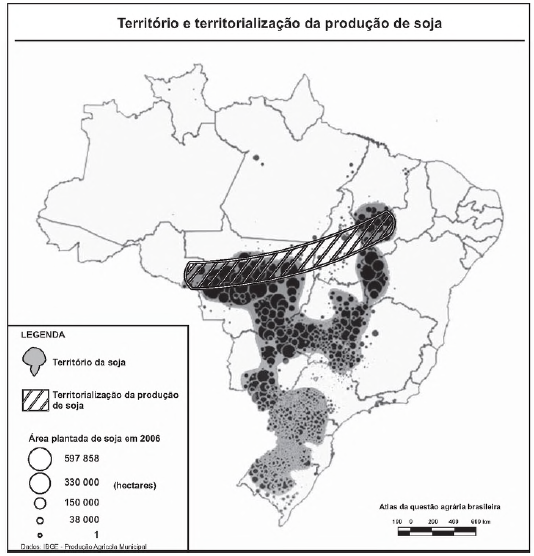
Inclusão de regiões com elevadas concentrações populacionais.
Incorporação de espaços com baixa fertilidade natural dos solos.
Integração com espaços de consolidação de reservas extrativistas.
Necessidade de proximidade física com os principais portos do país.
Reutilização de áreas produtivas decadentes da tradicional cultura canavieira.
Os desequilíbrios que se registram nas encostas ocorrem, na maioria...
aumento da atividade industrial.
crescimento populacional urbano desordenado.
desconcentração das atividades comerciais e dos serviços.
instalação de equipamentos urbanos na periferia da cidade.
construção de projetos habitacionais voltados à população de baixa renda.
Disponível em: www.fct.unesp.br. Acesso em: 1 ago. 2012. A...
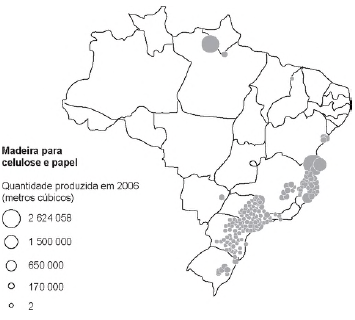
região produtiva contínua de perfil litorâneo.
integração intermodal entre Sul, Sudeste e Norte do país.
construção de eixos rodoviários entre as zonas produtoras.
organização da produção próxima às áreas de escoamento.
localização do setor nos limites das unidades político-administrativas.
Uma maior disponibilidade de combustível fóssil, como acontece com...
conquista da autossuficiência petrolífera pela descoberta de novas jazidas.
expansão da fronteira agrícola intensiva para produção de biocombustíveis.
superação do uso de energia não renovável no setor de transporte de cargas.
apropriação das condições naturais do território para diversificação das fontes.
redução do impacto social advindo da substituição de termelétricas por hidrelétricas.
Escoamento das águas das chuvas Disponível em:...
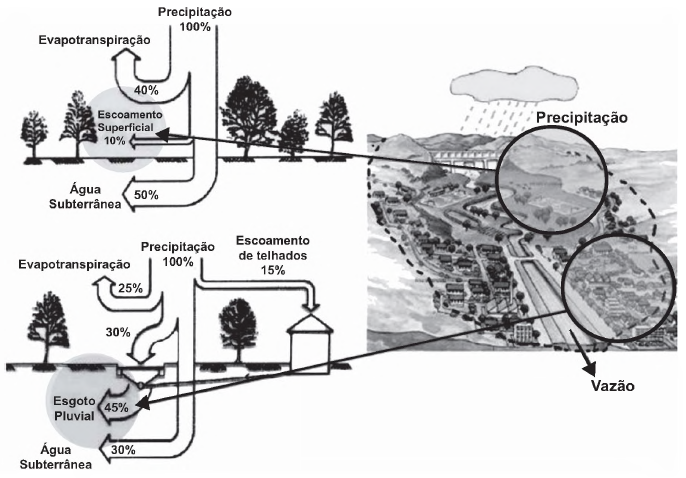
vazão hídrica nas estruturas artificiais construídas pelas atividades humanas.
Uma cidade que reduz emissões, eletrifica com energia solar seus...
tecnologia verde é necessária ao planejamento urbano.
mudança climática é provocada pelo crescimento das cidades.
consumo consciente é característico de cidades sustentáveis.
desenvolvimento urbano é incompatível com a preservação ambiental.
desenvolvimento social é condição para o desenvolvimento sustentável.
O uso intenso das águas subterrâneas sem planejamento tem causado...
O uso intenso das águas subterrâneas sem planejamento tem causado sérios prejuízos à sociedade, ao usuário e ao meio ambiente. Em várias partes do mundo, percebe-se que a exploração de forma incorreta tem levado a perdas do próprio aquífero.
TEIXEIRA, W. et al. Decifrando a Terra. São Paulo: Cia. Editora Nacional, 2009 (adaptado).
No texto, apontam-se dificuldades associadas ao uso de um importante recurso natural. Um problema derivado de
sua utilização e uma respectiva causa para sua ocorrência são:
Intrusão salina — Extração reduzida da água doce do subsolo.
Superexploração de poços — Construção ineficaz de captações subsuperficiais.
A voadeira, canoa de alumínio com motor de popa usada como meio de...
A voadeira, canoa de alumínio com motor de popa usada como meio de transporte fluvial pelos ribeirinhos da Amazônia, ganhou uma versão movida a energia solar em vez de combustível.
BRASIL, K. Voadeira movida a energia solar é opção para o transporte fluvial na Amazônia. Folha de S. Paulo, 12 maio 2012.
No texto, está descrita uma situação de mudança na
tecnologia do transporte fluvial na Amazônia. Configura-se
como uma consequência ambiental derivada da mudança
apresentada a redução
da área de mata ciliar.
da erosão dos solos aluviais.
de descargas elétricas nas águas.
do assoreamento dos cursos fluviais.
da emissão de poluentes atmosféricos.
A Estátua do Laçador, tombada como patrimônio em 2001, é um...

exemplo de bem imaterial.
forma de exposição da individualidade.
modo de enaltecer os ideais de liberdadade.
manifestação histórico-cultural de uma população.
maneira de propor mudanças nos costumes.
Canto dos lavradores de Goiás Tem fazenda e fazenda Que é grande...
atuação da bancada ruralista.
expansão da fronteira agrícola.
valorização da agricultura familiar.
manutenção da concentração fundiária.
implementação da modernização conservadora.
