Célula fotovoltaica: o que é e como funciona
As células fotovoltaicas são os menores constituintes dos sistemas geradores de energia elétrica que utilizam a energia solar como fonte primária. Os painéis solares que vemos nas casas, edifícios e satélites são compostos por conjuntos enormes dessas células.
Elas são feitas de um material semicondutor, geralmente silício dopado com átomos de boro ou fósforo, para possibilitar o efeito fotovoltaico, ou seja, a conversão da energia solar em eletricidade.
O efeito fotovoltaico é o fenômeno que ocorre quando a exposição de um material semicondutor à luz solar gera uma tensão elétrica no mesmo.
Células voltaicas
Uma célula fotovoltaica produz tipicamente uma potência elétrica da ordem de 1,5 W correspondente a uma tensão de 0,5 V e uma corrente de 3 A.
Para obter potências maiores, da ordem de 50 a 100W ou mais, as células são ligadas em série e/ou em paralelo, formando módulos e painéis fotovoltaicos.
Estrutura da célula fotovoltaica
A figura abaixo mostra a estrutura de uma célula fotovoltaica típica de Silício Policristalino.
A célula fotovoltaica possui uma forma aproximadamente quadrada com cerca de 15cm de largura.
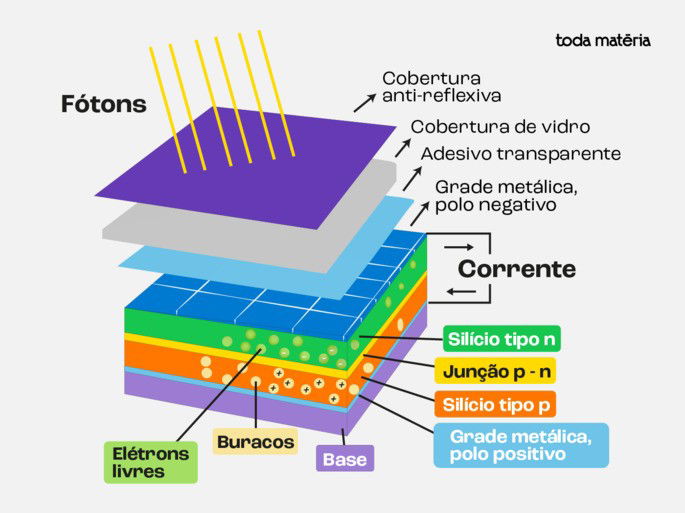
Os elementos principais são:
- Cobertura ou película antirreflexo de Nitreto de Silício: reduz a reflexão da radiação incidente para valores abaixo de 5%. Atente que sem este revestimento a célula refletiria cerca de um terço da radiação incidente.
- Grades metálicas e contatos frontais: são os terminais negativos da célula. São feitos de cobre.
- Camada de Silício tipo n: cristais de Silício dopados com átomos de Fósforo, constitui a região negativa da célula fotovoltaica. Sua espessura é aproximadamente 300 nm.
- Camada de Silício tipo p: cristais de Silício dopados com átomos de Boro, constitui a região positiva da célula fotovoltaica. Sua espessura é de aproximadamente 250 µm.
- Grades metálicas e contatos traseiros: são os terminais positivos das células.
O coração da célula fotovoltaica é o sanduíche composto pelas duas grades metálicas condutoras que envolvem as duas estruturas cristalinas de Silício - uma positiva por estar dopada com átomos de Boro (Silício tipo p), e outra negativa por estar dopada com átomos de Fósforo (Silício tipo n).
Estrutura microscópica da célula fotovoltaica
O átomo de Silício
O átomo de Silício é formado por 14 prótons e 14 elétrons. Na camada mais externa, conhecida como camada de valência, existem 4 elétrons.
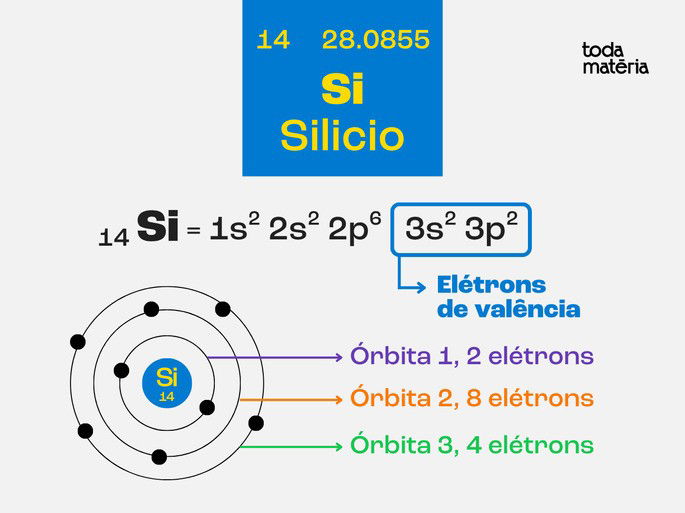
No cristal de Silício, os átomos organizam-se segundo uma estrutura que possibilita que os quatro elétrons da camada de valência formem quatro ligações covalentes com quatro átomos vizinhos.
Observe a figura abaixo onde estão representados apenas a última camada com os elétrons de valência em verde, e as ligações covalentes em vermelho.
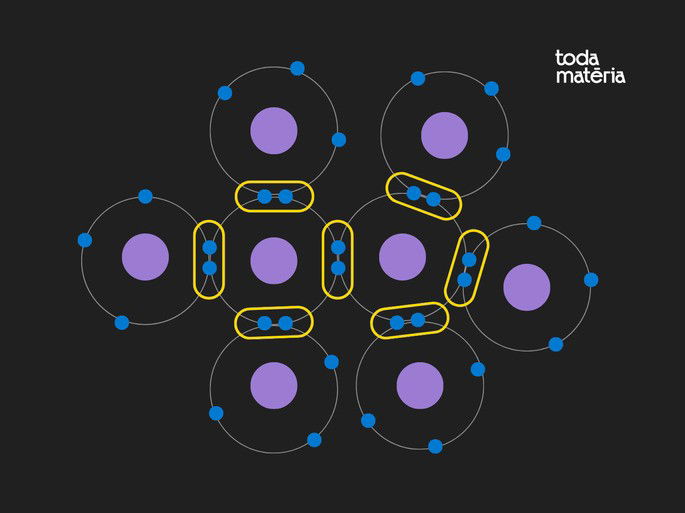
Observe que cada ligação covalente é formada pelos elétrons de valência de dois átomos vizinhos. Como resultado da partilha de elétrons, a banda de valência de cada átomo adquire mais quatro elétrons e fica completa, tornando o átomo estável. Isso porque a terceira camada do átomo de Silício comporta o máximo de 8 elétrons, distribuídos nos orbitais 3s e 3p.
Para que cada átomo consiga partilhar elétrons com quatro átomos vizinhos, a estrutura cristalina do silício não é coplanar, mas sim tridimensional, como representado na figura abaixo:
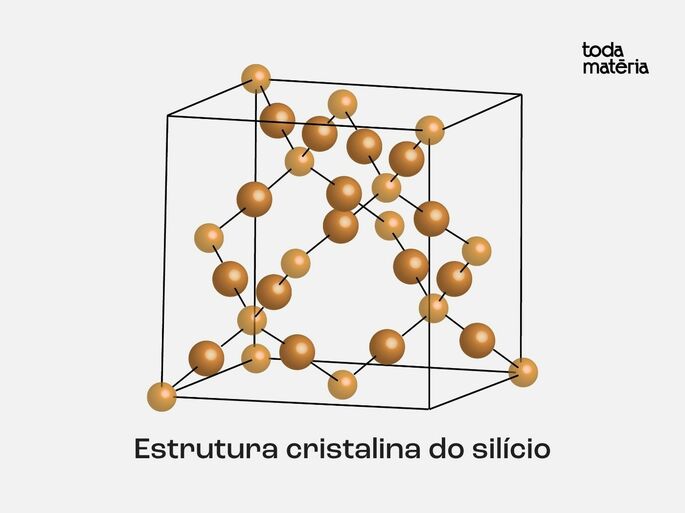
Como os átomos de Silício são estáveis na estrutura cristalina, existe uma diferença ou gap de energia entre suas bandas de valência e de condução.
Essa diferença é da ordem de 1,12 eV e representa a energia que o elétron de valência deve receber para saltar para a banda de condução.
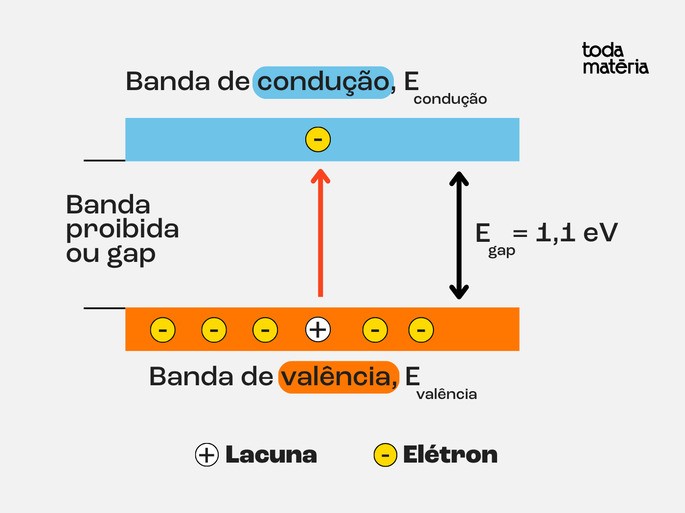
Quando um fóton de luz possui a energia de 1,12 eV, ele pode ser absorvido por um elétron da banda de valência do Silício, que salta para a banda de condução e deixa uma lacuna no seu lugar. Essa lacuna se comporta como uma carga positiva. Quando isso ocorre falamos que o fóton produziu um par elétron-lacuna.
Mas, o par elétron-lacuna produzido pelo fóton no cristal de Silício é instável e o elétron acaba por voltar para a banda de valência emitindo a energia absorvida.
Para gerar a corrente elétrica, é necessário que exista algo que impeça o elétron de voltar para a banda de valência. Isso é conseguido quando existe uma diferença de potencial (ddp) entre as duas partes constituintes da célula fotovoltaica.
Essa ddp é produzida pelo processo de dopagem do cristal de Silício com átomos de Boro e de Fósforo, pois a introdução desses átomos irá alterar as propriedades elétricas da estrutura cristalina do Silício.
O átomo de Boro irá fazer com que a estrutura cristalina do Silício adquira um caráter positivo e teremos a camada chamada Silício tipo p (p de positivo). Já o acréscimo de Fósforo irá fazer com que a estrutura adquira o caráter negativo e forme a camada chamada Silício tipo n (n de negativo).
Entre essas duas camadas, na junção p-n, irá existir um campo elétrico que impedirá que os elétrons que absorveram os fótons voltem para a banda de valência.
Dopagem da estrutura cristalina do Silício
Dopagem com Boro e o Silício tipo p
O átomo de Boro possui 5 elétrons, 2 na primeira camada e 3 na camada de valência.
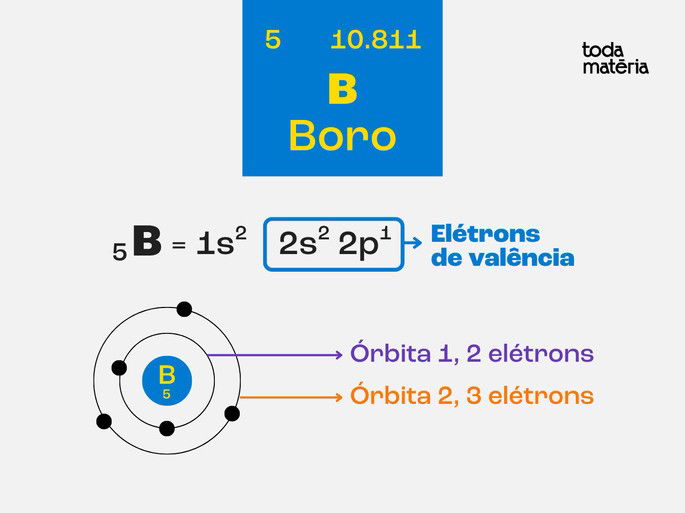
Quando inserido na estrutura cristalina do Silício, um átomo de Boro forma quatro ligações covalentes com quatro átomos vizinhos de Silício, mas como ele possui apenas três elétrons em sua banda de valência, existe a falta de um elétron.
Essa ausência é considerada uma lacuna que se comporta como uma carga positiva. O Boro é, então, o dopante usado para criar a região positiva ou tipo p na célula fotovoltaica.
Essa lacuna viaja através da estrutura até chegar na parte negativa da célula fotovoltaica, pois a cada vez que um elétron vizinho a preenche, outra lacuna surge.
A dopagem do Silício com Boro é feita na proporção de 1 átomo de Boro para cada 10 milhões de átomos de Silício.
Dopagem com Fósforo e o Silício tipo n
O átomo de Fósforo possui 15 elétrons, sendo 2 na primeira órbita, 8 na segunda órbita e 5 na terceira órbita que é a camada de valência.
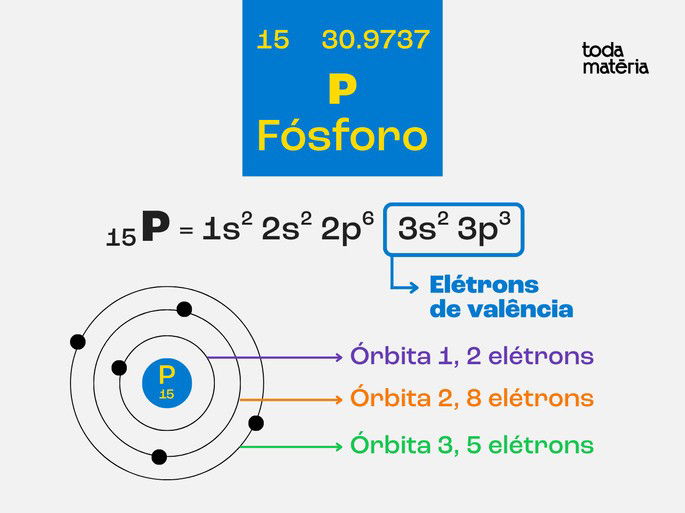
Quando inserido na estrutura cristalina do Silício, um átomo de Fósforo forma quatro ligações covalentes com os átomos vizinhos de Silício e deixa um elétron livre. Esse elétron livre pode se deslocar no material.
O átomo de Fósforo é usado, então, para criar a camada negativa no Silício, chamada tipo n. A razão entre átomos de Fósforo e de Silício é próxima de 1 para 1.000.
A junção p-n na célula fotovoltaica
A junção p-n é a região onde os dois tipos de Silício se encontram.
Essa região possui um campo elétrico que atua sobre os elétrons e lacunas, desviando-os para os terminais positivos ou positivos das grades e impedindo que eles voltem para a camada de valência.
Os elétrons que absorveram a energia dos fótons e saltaram das bandas de valência para as bandas de condução são acelerados para um terminal da grade, enquanto que as lacunas deixadas são enviadas para o outro terminal.
Nestas condições, irá surgir uma corrente elétrica quando os terminais da célula fotovoltaica forem ligados a um circuito que se fecha exteriormente.
O efeito fotovoltaico
Para entender o conceito do efeito fotovoltaico usamos a Teoria de Banda de Energia que diz que cada material possui até três bandas de energia, a de condução, a de valência e a proibida ou gap ou banda gap.
Materiais semicondutores, como o Silício, têm a banda de valência totalmente preenchida por elétrons e a banda de condução vazia em temperaturas da ordem de 20oC. A separação entre estas duas bandas de energia se dá pela banda proibida ou banda gap, que é da ordem de 1,12 eV nessa temperatura.
Quando o cristal de silício é sujeito à temperaturas de aproximadamente 200oC, a energia térmica fornecida é suficiente para excitar alguns elétrons da banda de valência para a banda de condução. Quando os elétrons saltam para a banda de condução, eles deixam lacunas positivas na banda de valência.
Na presença de um campo elétrico, tanto os elétrons quanto as lacunas transportam a corrente elétrica, conforme esquematizado na figura abaixo:
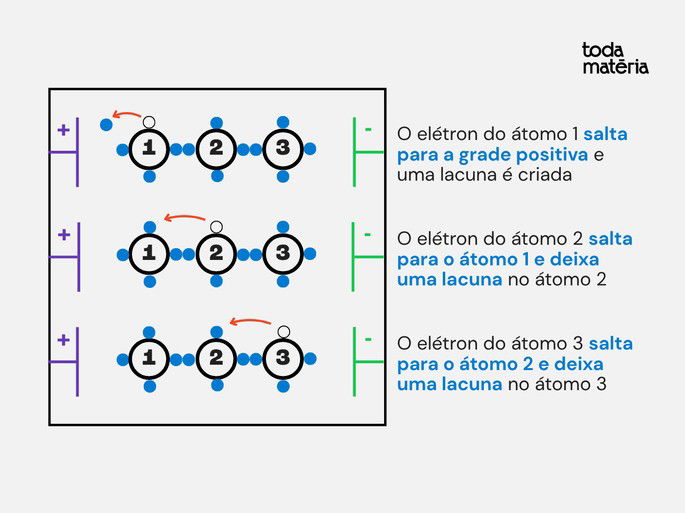
Observe na figura que se uma ligação covalente do átomo 1 for quebrada, aparecerá um elétron que será rapidamente atraído para o polo positivo (+), deixando em seu lugar uma lacuna.
Quando isso acontece um elétron pertencente a qualquer ligação covalente do átomo 2 poderá preencher a lacuna deixada pelo primeiro elétron do átomo 1. Quando o elétron abandona a ligação covalente do átomo 2, surgirá uma nova lacuna que, por sua vez, será preenchida por qualquer elétron de uma ligação covalente do átomo 3, e assim sucessivamente por toda a estrutura cristalina.
Influência da temperatura e da radiação incidente no funcionamento da célula fotovoltaica
Em condições normais de operação, os fabricantes indicam que as células fotovoltaicas apresentam um comportamento que varia com a temperatura e/ou com radiação da luz incidente.
Em relação à temperatura, os fabricantes anunciam que:
- A tensão de circuito aberto decresce com o aumento da temperatura;
- A potência máxima diminui com o aumento da temperatura;
- A corrente de curto-circuito varia muito pouco com a temperatura, sendo esta variação habitualmente desprezada.
- A potência de saída decresce com o aumento da temperatura.
Em relação à radiação incidente, os fabricantes atestam que:
- A tensão de circuito aberto pouco varia com a radiação incidente, sendo a variação mais significativa para valores mais baixos de radiação incidente;
- A potência máxima aumenta com o aumento da radiação incidente;
- A corrente de curto-circuito aumenta com o aumento da radiação incidente (varia aproximadamente de modo linear com a radiação incidente).
- A potência de saída aumenta com o aumento da radiação incidente.
Aplicações das células fotovoltaicas
As células fotovoltaicas são amplamente utilizadas em locais onde ocorre boa incidência de luz solar e onde o acesso à rede de energia elétrica é difícil. Abaixo listamos alguns usos:
- Nas áreas rurais: geração de energia elétrica para residências, bombeamento de água e irrigação.
- Complemento do abastecimento de energia elétrica de locais remotos com ou sem acesso à rede comum.
- Funcionamento de radares rodoviários móveis ou fixos.
- Iluminação de jardins e de áreas externas ou remotas.
- Fornecimento de energia para telefones de emergência, transmissores de TV e de celulares.
Abaixo mostramos um painel solar usado na iluminação pública:

Aprofunde os seus estudos:
Energia Solar: o que é, tipos e vantagens
Fontes Alternativas de Energia
Fontes de Energia: o que são e seus tipos (renováveis e não renováveis)
Referências Bibliográficas
Carneiro, J.A.O. Semicondutores : modelo matemático da célula fotovoltaica. Universidade do Minho, 2010. Acesso em 01/08/2025.
Castro, R.M.G. Introdução à Energia Fotovoltaica in Energias Renováveis e Produção Descentralizada. Universidade Técnica de Lisboa, 2002. Acesso em 01/08/2025.
Azevedo, M., Cunha, A. Fazer uma célula fotovoltaica. Escola Cooperativa Vale (S.Cosme) e Departamento de Física da Universidade de Aveiro. Acesso em 01/08/2025.
Célula fotovoltaica: o que é e como funciona. Toda Matéria, [s.d.]. Disponível em: https://www.todamateria.com.br/celula-fotovoltaica-o-que-e-e-como-funciona/. Acesso em:

